Почему ржавеет медь и как защитить ее от коррозии (видео)
Содержание:
- Осаждение бронзы из простого электролита без добавок.
- Негативное влияние меди на человека.
- Меры предосторожности
- Чистое железо
- В Minecraft начала окисляться медь и появились новые метрики
- Безопасные средства и инструменты для чистки меди
- Почему медные изделия требуется регулярно очищать?
- Отчего ржавеет нержавеющая сталь?
- Коррозионные свойства
- Нахождение в почве и влажном воздухе
- Как защитить медь от коррозии
- Способы окисления меди
- При каких условиях начинается разрушение алюминия на воздухе
- Химические свойства хрома
- Как алюминий защищен от коррозии?
- Физические свойства
Осаждение бронзы из простого электролита без добавок.
Невозможность осаждения бронз из простых ванн без добавок подтверждается экспериментально.На рисунке 4 показаны кривые циклической вольтамперометрии при осаждении из электролитов, содержащих медь, олово и одновременно медь с оловом. Добавки, кроме серной кислоты, и лиганды в электролит не вводились. Процесс велся на стальном вращающемся дисковом электроде при скоростях 0, 100 и 500 оборотов в минуту.
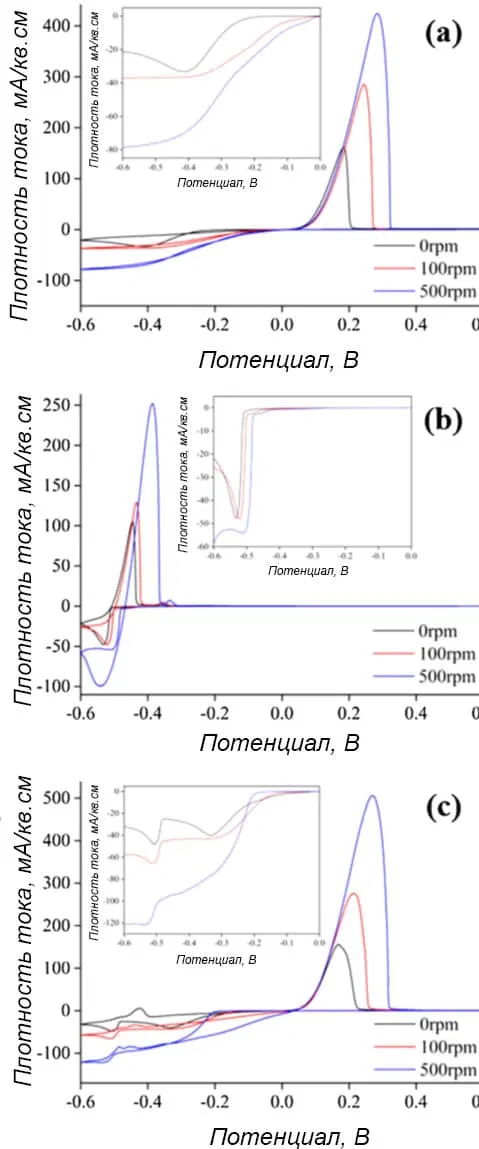
Рисунок 4- Циклические вольтамперограммы на стальном вращающемся дисковом электроде в электролитах: а — 0,1М CuSO4, b — 0,1М SnSO4, c — 0,1М CuSO4 + 0,1М SnSO4. Во всех случаях в электролиты вводили 1,4М H2SO4. Добавки не применялись.
На кривых точно видны два потенциала: начала восстановления и анодного растворения указанных металлов. Восстановление Cu2+ до Cu начиналось в диапазоне от -0,017 до -0,112 В, в зависимости от скорости вращения электрода (рисунок 4а). При анодной поляризации наблюдались одиночные скачки тока, появляющиеся при 0,05 В и имеющие разные площади пиков.
В случае олова (рисунок 4b) потенциал начала восстановления находился в диапазоне от -0,464 до -0,414 В, в зависимости от скорости вращения электрода. После начала процесса плотность тока скачкообразно возрастала при -0,5 В и впоследствии уменьшалась. При совместном присутствии в электролите меди и олова без добавок (рисунок 4c) первый потенциал начала восстановления меди составлял -0,022 В при 0 об/мин, -0,134 В при 100 об/мин и -0,196 В при 500 об/мин. Предельный ток достигался при -0,48В. При дальнейшей катодной поляризации от -0,5В плотность тока снова увеличивалась, что говорило о начале восстановления олова. Таким образом, в смешанном растворе на катодных ветвях вольтамперограммы обнаруживались два четко разделенных скачка тока, характеризующих восстановление меди и олова. Это означает, что соосаждения их не было и бронза не образовывалась.
Поскольку медь предпочтительнее восстанавливается из-за ее более положительного стандартного потенциала, в электролите без добавок и лигандов на катоде меди осаждалось гораздо больше, чем олова. Это согласуется с профилем сканирования в режиме анодной поляризации. Большие пики анодного растворения обнаруживались в диапазоне от 0,18 до 0,28В в электролите, содержащем только медь (рисунок 4а), и от -0,44 до -0,38В в электролите, содержащем только олово (рисунок 4b). В смешанном же растворе наблюдались очень маленькие пики между -0,45 и -0,42 В и большой пик при 0,167 В. Таким образом, это является еще одним доказательством того, что электрохимическое восстановление в смешанном растворе Cu/Sn в основном приводит к осаждению меди.
Негативное влияние меди на человека.
Избыток меди в организме как правило возникает у людей работающих на вредных производствах. Например, во время шлифовки медного изделия в воздух рабочей зоны в виде пыли попадают частицы меди и её оксида. Концентрация их может достигать от 0,3 до 15 мг./м3. Примерно через час вдыхания такого воздуха рабочим начнет ощущаться сладковатый привкус во рту, затем возникнет кашель, а если не предпринять никаких действий и продолжить работу, то спустя ещё несколько часов появятся такие симптомы как тошнота, головная боль, повышенная температура.
Интоксикация медью также может наступить при длительном проживании в экологически неблагоприятных районах, неправильном использовании лекарственных препаратов, чрезмерном употреблении в пищу некоторых продуктов.
Медь в продуктах питания может присутствовать как в естественных концентрациях, так и копиться искусственно. Например, рыба может жить в водоемах, загрязненных медью от сбросов сточных вод с превышением ПДК по меди. Оттуда же может пить скот. В конечном счете рыба, мясо и субпродукты попадут на стол к человеку, но качество их будет низким, а количество меди будет зашкаливать.
Каковы последствия интоксикации медью?
а. Угнетение нервной системы.
В высоких концентрациях медь оказывает крайне негативное влияние на работу ЦНС. вплоть до развития болезни Альцгеймера.
б. Инактивация ферментов.
При избытке меди в организме происходит снижение активности образования, либо полная инактивация некоторых ферментов.
в. Угнетение дыхания.
Замедляется поступление кислорода в клетки крови, появляется головная боль, затрудняется дыхание, учащается серцебиение, возникает тревожность. Возможно развитие диареи, тошноты, болей в животе и сильного увеличения печени.
При хроническом отравлении медью может возникать такой парадокс — избыточные ионы меди начнут откладываться в различных тканях (почки; радужные оболочки глаз; печень) оказывая на них токсичное воздействие, хотя в нормальной цепи процесса обмена веществ организма возникает дефицит этого микроэлемента.
Меры предосторожности
Большинство способов очистки меди представляют собой угрозу здоровью человека, а потому требованием безопасности является наличие специальной одежды, резиновых перчаток, респиратора и по возможности очков. Не рекомендуется оставлять открытые участки кожи. Требуется обеспечить хорошую вентиляцию, так как пары того же уксуса могут повредить дыхательные пути.
Нельзя склоняться над реагентом, в особенности если идет яркая реакция, поскольку могут лететь брызги, которые повредят кожный покров, а также едкие испарения вредят органам дыхания. Чтобы не поцарапать изделие, которое требует очищения, рекомендуется использовать мягкие материалы без высоких абразивных свойств.
Не рекомендуется передерживать в растворе предмет больше требуемого для очистки времени, поскольку в этом случае растворен будет не только оксид, но и сам предмет. Не стоит подвергать опасности древние монеты и статуэтки, поскольку повредить эти предметы проще всего. Рекомендуется проверить метод чистки на небольшом участке, либо уже испорченной вещи, чтобы оценить средство. Только в случае, если с предметом не произошло ничего плохого, стоит использовать его на всем предмете.
Чистое железо
Чистое железо (Fe): серебристый металл белого цвета, проявляющий амфотерные свойства (то есть может вступать в реакцию с кислотами и щелочами). Железо — металл тяжёлый (1 м3 весит 7800 кг), имеет высокую пластичность и прочность (прочнее меди). Чистое железо — металл с содержанием чистого железа по массе около 99,995%, — практически не применяется. Говоря о железе, обычно подразумевают его сплавы с углеродом и другими элементами: до 2,14% углерода – это стали, более 2,14% – чугуны. При наличии других элементов и изменении их концентрации в железном сплаве (стали) резко меняются физико-механические свойства сплава.
Если концентрация углерода в сплаве железа превысит 6,67%, то углерод вступит в химическую реакциюс железом, образовав уже не сплав, а химическое соединение — карбид железа FeC2.
Чистое железо плавится при температуре 1540°С, пластично, легко поддаётся намагничиванию. При нагревании до 768°С железо теряет свои магнитные свойства.
Чистое железо — химически активный элемент. Железо и соляная кислота легко реагирует друг с другом, образуя хлорид железа FeCl2. Чистое железо легко окисляется даже во влажном воздухе, образуя триокись железа Fe2 O3*nH2O, по-другому называемая ржавчиной. Железо и серная кислота реагирует с образованием сульфата железа Fe(SO4)2, — прозрачного зеленоватого раствора. Если оставить раствор на воздухе, то можно заметить через некоторое время образование бурого осадка,- это сульфат железа соединился с кислородом воздуха, образовав рыхлую бурую массу нового соединения железа: Fe(SO4)3
Азотная кислота и чистое железо реагируют с образованием нитрата железа Fe(NO3)2, окиси азота NO или аммиачной селитры NH4NO3 (вещество ещё известное в качестве аммиачного удобрения) и воды.
Так реагируют разбавленные кислоты с железом. Концентрированная азотная и серная кислоты на чистое железо не действуют (при комнатной температуре), благодаря наличию образующейся оксидной плёнки.
Железо легко вытесняет медь в химической реакции замещения, если в раствор медного купороса опустить металлическое изделие. Мы будем наблюдать на поверхности железа образование микроскопических кристаллов химически чистой меди красно-бурого цвета.
При этом голубой раствор медного купороса постепенно бледнеет и приобретает зеленоватый окрас, происходит образование железного купороса FeSO4x5H2O.
Но это способ не эффективен для прочного медного покрытия. Для более качественного нанесения медного покрытия используют электричество. Таким способом (реакцией замещения) можно покрыть медью любой металл, стоящий левее меди в ряду напряжений.
Но необходимо помнить, что в случае образования глубоких царапин по поверхности покрытия, могут образовываться (если система находится в электролите) гальванические элементы, что приводит к разрушению металлов.
Чистое железо придаёт окрас некоторым минералам: гематит (от серого до тёмного тона окраски), топаз (бесцветный, синий голубой, жёлтый, оранжевый).
Наиболее важными химическими соединениями железа являются:
FeSO4x5H2O — железный купорос — применяется в сельском хозяйстве как яд для борьбы с вредителями;
Fe2(SO4)3x9H2O — водный сульфат железа применяется для очистки воды;
FeCl3 — также применяется для очистки воды, а также для травления меди (электроника)
Fe(NO3)2x9H2O — водный нитрат железа — применяется в текстильной промышленности для обработки и покраски ткани
Что касается чистого железа, то оно используется, в основном, как катализатор в химических реакциях.
Определить наличие ионов железа (2-х или 3-х валентного) можно с помощью
Железо образует 3 различных , отличающихся степенью окисления железа и цветом химического соединения и его активностью.
В Minecraft начала окисляться медь и появились новые метрики
Подземелья, конечно, тоже еще раз изменились, но генератор почти не трогали.

Java-версия Minecraft получила снапшот 21W11A, вводящий еще немного изменений из обновления Caves & Cliffs. По сравнению с изменениями предыдущих недель снапшот скромный: в основном он сфокусирован на исправлении ошибок.
Самое заметное визуальное изменение версии 21W11A это окисление меди. Со временем медные блоки будут менять цвет, превращаясь из коричневых в зеленые; вот так выглядят стадии патинирования блоков.

Эффект чисто визуальный, по характеристикам патинированный медный блок не отличается от обычного. Чтобы очистить блок от патины, можно воспользоваться топором или дождаться, пока в блок ударит молния. Кстати, громоотводы теперь можно частично погружать в воду.
Кроме того, теперь медные блоки можно вощить прямо в игровом мире: для этого достаточно кликнуть правой кнопкой мышки по такому блоку, удерживая в руках пчелиные соты. Вощеный медный блок не окисляется, его можно превратить в четыре медных слитка. Уже нанесенный воск убирается с помощью все того же топора.
В снапшоте снова перенастроили генератор пещер, немного изменив их размеры. Блоки алмазной руды теперь будут встречаться немного чаще; совместив блок мха с плитой или камнем, игроки получат мшистые версии этих блоков.
Также в 21W11A появились новые метрики производительности. Если во время игры нажать комбинацию F3 + L, то клиент будет на протяжении 10 секунд записывать время обсчета тиков, нагрузку на память и множество других технических данных.
Эта информация сохраняется в специальном файле, расположенном в директории debug/profiling. Игроки могут использовать ее для отладки собственных проектов или прикладывать к сообщениям об ошибках.
Источник
Безопасные средства и инструменты для чистки меди
Чтобы правильно подобрать метод очищения меди в домашних условиях, следует определить, есть ли на изделии налет из окиси или оно покрыто лаком. Для этого на потемневшее место нужно нанести небольшое количество смеси из соды и уксусной кислоты. Если обработанная область быстро посветлеет и начнет блестеть, значит, изделие не покрыто лаком и нуждается в очищении. Если же защита присутствует, достаточно помыть медный предмет теплой мыльной водой.
Зеленый налет на меди выделяет токсины, а чистящие средства могут быть вредны для здоровья, поэтому начиная чистку изделий, следует позаботиться о собственной безопасности. Необходимо приготовить резиновые перчатки, защитные очки и ватно-марлевую повязку.
Самые бережные средства
Ценные медные изделия, такие как монеты или антиквариат, необходимо очищать очень осторожно, используя средства, которые не оставляют царапин и не портят поверхность. Можно применить:
- 10% раствор из лимонной кислоты, который поможет бережно убрать любой налет с медной поверхности.
- Кефир или кетчуп. Кислые продукты хорошо растворяют налет. Загрязненный предмет поместить в любой ингредиент на несколько часов, после чего помыть под проточной водой.
- Мыльный раствор. Натертое хозяйственное или детское мыло залить кипятком. Затем медную вещь поместить в него на несколько часов.
Последний способ занимает много времени. Сильные загрязнения им с первого раза не удалить. Зато он бережный и не повредит ценное изделие.
Химические средства для чистки медных изделий
Очищая медь от зеленоватого налета химией, не стоит использовать абразивные вещества, которые могут поцарапать поверхность. Лучше приобретать препараты, предназначение для драгоценных и цветных металлов, которые выпускаются в виде гелей и пасты.
Названия некоторых средств для чистки меди:
- Unicum – гелеобразный препарат, с помощью которого можно восстановить изначальный вид металла и вернуть ему блеск. Не оставляет царапин и легко удаляет загрязнения.
- Centralin – паста, которая за короткое время очищает медные изделия, возвращает им блеск и образует защитную влагоотталкивающую пленку.
- Delu Kupferfix polish – бережно очищает медную поверхность, защищает от потускнения и удаляет загрязнения.
- Sambol – мягко и тщательно чистит изделия. Убирает грязь и окисления, не повреждая поверхность. Восстанавливает блеск и защищает от потемнения.
Прежде чем использовать препарат, следует испробовать его на небольшой поверхности медного изделия. Если металл не реагирует, продолжать чистку.
Народные средства для удаления налета с меди
Почистить медные изделия можно подручными веществами, которые дешевле и безопаснее для организма, чем химия. Вот несколько простых рецептов:
- Гель для мытья посуды. Помогает почистить предметы с небольшими загрязнениями. Изделие обрабатывается мягкой губкой с нанесенным на нее средством. После ополаскивается под проточной водой.
- Лимон. Медная поверхность натирается половинкой цитруса. Для большего эффекта прочищается ворсистой упругой щеткой.
- Уксус и мука. Вернуть изначальный блеск можно с помощью средства, которое в народе называется «уксусное тесто». В равных пропорциях смешивается пшеничная мука и уксусная кислота. Смесь наносится на изделие и оставляется до полного высыхания. Образовавшаяся корка легко оттирается, поверхность отполировывается мягкой тканью.
- Нашатырный спирт. Чтобы убрать зеленый налет и почернение, изделие обрабатывается нашатырем и тщательно ополаскивается под проточной водой.
- Соль и уксусная кислота. В слабом растворе уксуса растворяется 2 ст. л. соли. В емкость помещается очищаемая вещь и кипятится 10 мин. Затем на некоторое время изделие опускается в чистую воду, после чего протирается насухо мягкой тканью.
Применяя любой из методов, необходимо придерживаться правил безопасности.
Почему медные изделия требуется регулярно очищать?
Ковши из меди, турки, самовары отличаются высокой степенью тепловой проводимости, и потому нагревание в них протекает равномерно, а продукты будут приготовлены быстрее. Это обусловлено высокую популярность изделий в быту. Потребность в очистке медных предметов обусловлено утратой ими визуальной привлекательности спустя время. Особенно быстро начинают тускнеть и теряют естественный цвет изделия, которые находятся на воздухе или даже часто нагревающиеся.
Коррозия меди в виде оксидной пленки (патины) популярна лишь в тот момент, где требуется придание предметам винтажного облика, стилизация под старину. В обратном случае она будет портиться внешний вид посуды, утвари, а также статуэток и украшений. Чтобы устранять оксидный налет, элементы потемнения и вернуть прежний блеск, требуется время от времени чистить предметы. Также очищение требуется для того, чтобы исключить попадания в пищу вредоносных соединений, которые способы присутствовать в зеленом и черном слое.
Эффективные способы очистки меди
Произвести очищение медных предметов несложно, для этого не требуются дорогостоящие средства. Вот наиболее популярные методики, которые используют в домашних условиях:
- Кетчуп – возьмите немного кетчупа из томатов, смажьте им изделие и оставьте на пару минут. После сполосните струей чистой и прохладной воды.
- Раствор для мытья посуды – следует намылить хозяйственную губку простым средством для посуды, тщательно протирайте поверхность и смывайте водой. такой метод лучше всего подойдет для изделий, которые лишь слегка потускнели.
- Лимон – следует натереть медную поверхность лимонной долькой, а после пройдитесь по нему щеточкой с жесткими ворсинками и помойте водой.
- Мука и уксус – влейте в чашку малое количество, добавьте муки до получения теста со средней густотой. Смажьте медное изделие посредством теста, оставьте до просыхания, а после удалите остатки. После остается натереть изделия мягкой тряпкой.
- Соль и уксус – налейте в кастрюльку из нержавеющей стали уксус 9%, всыпьте немного соли и доведите до кипения. Огонь следует выключить, закинуть в раствор предмет из меди, не убирать его до остывания жидкости. Данный способ подойдет для очень загрязненных поверхностей.
А теперь рассмотрим, как чистить медные монеты.
Очистка медных монет
Следует помнить о том, что иногда слой патины помогает придавать монетам более винтажный и благородный внешний вид, и потому удалять его стоит не всегда. Некоторые де стараются искусственно состарить деньги домашним методом. Для этого возьмите литр дистиллированной воды, 5 грамм марганцовки (аптечной) и 50 грамм медного купороса. Раствор следует нагреть, не доводя до кипения, бросить в него монеты, оставить до получения требуемого оттенка. Для закрепления полученного эффекта просохшие деньги обработайте все смесью спирта и бензола (1 к 1). После монеты обретают красивый состаренный вид и способны украшать любые коллекции антикварных предметов.
Источник
Отчего ржавеет нержавеющая сталь?
Название «нержавеющая сталь» как бы подразумевает, что перед нами – сталь, которая не ржавеет. Однако вот лежат на заброшенной стройке ржавые трубы (из нержавеющей стали), вот стоит на свалке ржавый «Запорожец» (из нержавеющей стали), а где-нибудь под ванной можно отыскать случайно потерянное бритвенное лезвие – ржавое-ржавое, зато с гордой надписью «stainless steel»(«нержавеющая сталь»). В чём же дело?
У побережья Италии, в заливе Таранто, археологи обнаружили остатки корабля, затонувшего в далёком 180 году нашей эры. Анализ обломков показал, что виновником древней катастрофы стали проржавевшие железные гвозди, которыми была приколочена к днищу судна деревянная заплата. Скорее всего, во время внезапно налетевшей бури ржавые гвозди не выдержали, заплата отвалилась и корабль пошёл ко дну с грузом и экипажем – всего в 500 метрах от берега.
Как видите, уже 2000 лет назад люди сталкивались с трагическими последствиями «коррозии металла» – от латинского слова «corrodere», то есть «грызть, разъедать»). Ржавчина стала причиной многих трагедий – например, в 1967 в США из-за вызванной коррозией трещины в подвесном стержне обрушился Серебряный Мост через реку Огайо. В катастрофе погибло 46 человек!
С точки зрения химии ржавчина – это оксид железа-три, соединение железа с кислородом. Кислород (O), содержащийся в воздухе, воде или кислотах, активно реагирует с атомами железа (Fe), образуя оранжево-красный оксид (с формулой Fe2O3)
Если вы когда-нибудь видели природные источники железистых минеральных вод, например, знаменитого нарзана, то наверняка обращали внимание на оранжевый цвет земли и камней рядом – это в точности та же самая ржавчина, соединение железа с кислородом. На поверхности железного или стального предмета ржавчина не останавливается – она продолжает распространяться вглубь, пока предмет не проржавеет насквозь. Что же такое «нержавеющая сталь»? Это сплав железа и углерода с примесью другого металла – хрома
Кислород соединяется с хромом более активно, чем с железом. Хром для кислорода «вкуснее» железа – в результате образуется тонкая невидимая плёнка окиси хрома, абсолютно непроницаемая для кислорода. В итоге сталь оказывается надёжно защищённой от коррозии
Что же такое «нержавеющая сталь»? Это сплав железа и углерода с примесью другого металла – хрома. Кислород соединяется с хромом более активно, чем с железом. Хром для кислорода «вкуснее» железа – в результате образуется тонкая невидимая плёнка окиси хрома, абсолютно непроницаемая для кислорода. В итоге сталь оказывается надёжно защищённой от коррозии.
«Но почему же она тогда всё-таки ржавеет?» – спросите вы. Причин – две. Первая – хрома может оказаться недостаточно, такая ситуация может возникнуть при контакте нержавеющей стали с обыкновенной углеродистой сталью. Именно поэтому инструкции категорически запрещают контакт деталей из «нержавейки» с деталями из обычной стали – нержавейка начнёт ржаветь. Вторая причина – защитная плёнка не является какой-то суперпрочной, её можно повредить. Она легко разрушается кислотами или соединениями йода, фтора и хлора. Морская вода или чистящие средства, содержащие хлор («Доместос гель», «Белизна» и так далее) – страшные враги нержавеющей стали! Даже обычная дождевая вода для нержавеющей стали опасна – потому что в каплях дождевой воды всегда содержится небольшое количество угольной кислоты (H2CO3).
Таким образом, нержавеющая сталь не будет ржаветь только в том случае, если за ней постоянно и бережно «ухаживают» – чистят (средствами, не содержащими хлор!), вытирают насухо, покрывают лаком или краской и так далее. А вот если предмет из «нержавейки» просто бросить на улице, как тот же старый автомобиль, рано или поздно краска облупится, кислота разъест защитную плёнку, и железо начнёт превращаться в ту самую ржавчину со всеми вытекающими последствиями. «По ржавому ножу узнаёшь нерадивого хозяина» – говорит восточная поговорка. Так и есть!
Коррозионные свойства
В сухом воздухе образуется тонкая оксидная пленка, толщина которой составляет около 50 нм. В пресной воде скорость коррозии металла составляет 0,05–0,25 мм/год. Однако при содержании в жидкости аммиака, сероводорода, хлоридов и некоторых других примесей интенсивность коррозионного процесса возрастает.
В морской воде коррозия меди незначительна, и интенсивность ее соизмерима с разрушением в пресной. Однако при увеличении скорости движения среды возникает ударная коррозия, что приводит к повышению скорости процесса. Коррозия меди существенно зависит от температуры, и при возрастании последней скорость разрушения увеличивается.
Медь является единственным материалом, который не подвержен обрастанию водорослями, так как ее ионы губительно действуют на них. В почве, насыщенной микроорганизмами, скорость коррозионных процессов заметно возрастает. Интенсивность их протекания напрямую зависит от pH грунта. Чем больше отклонение значения показателя от нейтрального, тем быстрее происходит коррозия металла. Влияние микроорганизмов на процесс разрушения обуславливается выделением сероводорода в результате их жизнедеятельности.
Продукты почвенной коррозии элемента отличаются от атмосферной, имеют более сложный состав и структуру.
Коррозия меди, покрытой слоем олова (луженой), практически отсутствует. При качественном лужении она прекрасно служит под воздействием града и снега, становится нечувствительной к перепаду температур. Срок службы таких материалов составляет около 100 лет. При этом не теряются первоначальные свойства. Со временем цвет не изменяется, а остается первоначальным — серебристо-металлическим. Луженая медь прекрасно показала себя в качестве кровельного материала. Ведь не зря купола многих храмов покрывают именно этим материалом.
Медь хорошо зарекомендовала себя в кровле.
Из-за высокой коррозионной устойчивости к воздействию многих агрессивных сред медь нашла широкое применение в химической промышленности.
Устойчивый металл широко используется в химической промышленности.
В гальванической паре она является катодом для большинства металлов и сплавов и в результате электрохимических процессов при контакте с ними вызывает их ускоренную коррозию.
Нахождение в почве и влажном воздухе
Коррозия меди в почве, в основном, вызывается влиянием кислот, которые содержатся в грунте. Если сравнить с воздействием воды, то кислород в грунте значительно меньше окисляет металлические элементы. К наиболее опасным в почве относятся микроорганизмы, вернее, их выделения. Зачастую они способны выделять сероводород, разрушающий металл. Так, медь длительно пролежавшая в почве способна полностью разложиться.
Во влажном воздухе процесс протекает не стремительно. Необходимо длительное время. В сухом климате можно вообще не наблюдать разрушительных влияний. Объясняется это тем, что во влажном воздухе высока концентрация углекислого газа, сульфидов, хлоридов, вызывающих коррозию и разрушительных для защитной пленки.
Длительное пребывание на влажном воздухе способно вызывать образование слоя патины. Так называется зеленый налет на меди. Она представляет собой оксиды солей, которые на начальном этапе темно-коричневого цвета, а затем поверхность начинает зеленеть. Особенностью патины является то, что ее невозможно растворить в воде и на нее не действует повышенная влажность воздуха. Она имеет нейтральные свойства к самой меди, что позволяет ей защищать поверхность от пагубного влияния окружающей среды. Кроме этого современные методы создания искусственной патины позволяют ее использовать в предметах искусства и при реставрации.
Посмотрите личный опыт борьбы с коррозийными очагами с помощью ингибиторов.
Как защитить медь от коррозии
Существует множество средств, которые позволяют уменьшить вероятность появления коррозии в различных средах. Среди них такие, как:
Изменение состава материала. Использование легирования позволяет значительно увеличить уровень коррозийной стойкости. При этом примеси могут быть разные – главное учитывать область использования готовой детали и понимать потенциальные риски, чтобы их устранить.
Лужение. Процесс заключается в обработке жидким оловом. На поверхности создается эффективный защитный слой. При условии отсутствия дефектов, он ограничит контакт с атмосферой и другими факторами, приводящими к появлению коррозии.
Контроль за областью использования
При закупке медных изделий важно понимать, где вы будете их применять. Требуется оградить материал от контакта с серой и ее соединениями, не допустить, чтобы поблизости располагались цинковые или алюминиевые детали
Они могут спровоцировать появление электрохимической коррозии.
Учет стандартных требований по использованию медных изделий позволит значительно увеличить срок их службы и не допустить проблем с возникновением коррозии. Вернуться к статьям Поделиться статьей
Способы окисления меди
Как ведет себя металл при контакте с воздухом
Окисление меди — естественный процесс. В периодической таблице Д. И. Менделеева медь расположена в группе «Металлы» под номером 29. Как и остальные металлы, она способна окисляться и образовывать устойчивые соединения в виде окисей и солей. Чтобы понять, что же такое окись меди, стоит приглядеться к старой бронзовой статуе. Со временем фигурка становится светло-зеленой из-за окисленной меди в составе бронзы. «Свежеизготовленная» бронзовая статуя окрашена в кирпичный цвет, но спустя время под действием влажного воздуха и углекислого газа протекает такая реакция:
Полученное сочетание соли и гидроксида меди — это малахит. Из него делают краски и всевозможные украшения.
Окислить медные изделия можно различными способами. В промышленности проводят анодное окисление с помощью электродов. Этот сложный и дорогостоящий процесс требует специального оборудования. В домашних условиях окислять медь гораздо проще.
При каких условиях начинается разрушение алюминия на воздухе
Вам будет интересно:Альтернативность — это наличие выбора возможностей
Некоторые интересуются, ржавеет ли алюминий на воздухе. Если будет разрушена оксидная пленка на верхнем слое металла, то может начаться процесс коррозии. В результате может проявиться ржавчина. Рост пленки, как правило, замедляется на свежем воздухе. Следует помнить, что оксид алюминия отличается хорошей сцепкой с поверхностью металла.
Если лист хранится на складе, то пленка будет от 0,01 до 0,02 мкм. Если металл соприкасается с сухим кислородом, то толщина оксидной пленки на поверхности будет от 0,02 до 0,04 мкм. Если алюминий подвергают термической обработке, то толщина пленки изменяется. Она будет равна 0,1 мкм.
Считается, что алюминий обладает достаточной стойкостью, чтобы использовать его на свежем воздухе. Например, его применяют в сельской местности, а также в удаленных промышленных зонах.
Химические свойства хрома
Хром — элемент VIB группы таблицы Менделеева. Электронная конфигурация атома хрома записывается как 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1 , т.е. в случае хрома, также как и в случае атома меди, наблюдается так называемый «проскок электрона»
Наиболее часто проявляемыми степенями окисления хрома являются значения +2, +3 и +6. Их следует запомнить, и в рамках программы ЕГЭ по химии можно считать, что других степеней окисления хром не имеет.
При обычных условиях хром устойчив к коррозии как на воздухе, так и в воде.
Взаимодействие с неметаллами
с кислородом
Раскаленный до температуры более 600 o С порошкообразный металлический хром сгорает в чистом кислороде образуя окcид хрома (III):
с галогенами
С хлором и фтором хром реагирует при более низких температурах, чем с кислородом (250 и 300 o C соответственно):
С бромом же хром реагирует при температуре красного каления (850-900 o C):
с серой
С серой хром может образовывать как сульфид хрома (II) так и сульфид хрома (III), что зависит от пропорций серы и хрома:
С водородом хром не реагирует.
Взаимодействие со сложными веществами
Взаимодействие с водой
Хром относится к металлам средней активности (расположен в ряду активности металлов между алюминием и водородом). Это означает, что реакция протекает между раскаленным до красного каления хромом и перегретым водяным паром:
Взаимодействие с кислотами
Хром при обычных условиях пассивируется концентрированными серной и азотной кислотами, однако, растворяется в них при кипячении, при этом окисляясь до степени окисления +3:
В случае разбавленной азотной кислоты основным продуктом восстановления азота является простое вещество N2:
Хром расположен в ряду активности левее водорода, а это значит, что он способен выделять H2 из растворов кислот-неокислителей. В ходе таких реакций в отсутствие доступа кислорода воздуха образуются соли хрома (II):
При проведении же реакции на открытом воздухе, двухвалентный хром мгновенно окисляется содержащимся в воздухе кислородом до степени окисления +3. При этом, например, уравнение с соляной кислотой примет вид:
При сплавлении металлического хрома с сильными окислителями в присутствии щелочей хром окисляется до степени окисления +6, образуя хроматы:
Как алюминий защищен от коррозии?
Сплавы других металлов подвержены появлению ржавчины. Она проявляется достаточно быстро. Если создать для алюминия определенные условия, то он не будет разрушаться долгие годы. Для защиты алюминия от коррозии на нем образуется специальная пленка. Она ложится тонким слоем, который составляет от 5 до 10 миллиметров. Состоит подобное покрытие из оксида алюминия.
Пленка является прочной и дает металлу дополнительную защиту от внешних негативных воздействий. Благодаря такому слою воздух и влага не попадают в структуру материала. Если целостность оксидного покрытия нарушается, то начинается процесс коррозии алюминия. Металл теряет свои свойства.
Физические свойства
- Плотность — 8500—8700 кг/м³.
- Удельная теплоёмкость при 20 °C — 0,377 кДж·кг−1·K−1.
- Удельное электрическое сопротивление — (0,07-0,08)·10−6 Ом·м .
- Температура плавления латуни в зависимости от состава достигает 880—950 °C. С увеличением содержания цинка температура плавления понижается. Латунь достаточно хорошо сваривается различными видами сварки, в том числе газовой и дуговой в среде защитных газов, и прокатывается. Технологии сварки латуни описаны в соответствующей литературе. Хотя поверхность латуни, если не покрыта лаком, чернеет на воздухе, но в массе она лучше сопротивляется действию атмосферы, чем медь. Имеет жёлтый цвет и отлично полируется.
- Висмут и свинец имеют вредное влияние на латунь, так как уменьшают способность к деформации в горячем состоянии. Тем не менее легирование свинцом применяют для получения сыпучей стружки, что облегчает её резку.